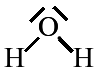
H2O
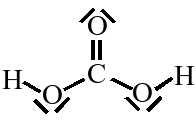
H2CO3
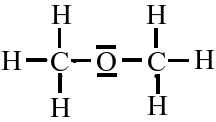
C2H6O
(mind. 2 verschiedene!)
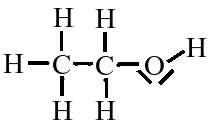
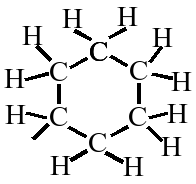
C6H12
(mind. 2 verschiedene!)
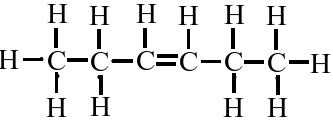
C2H2
![]()
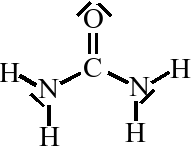
CH4N2O
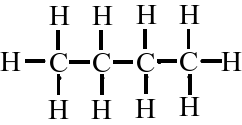
C4H10
(mind. 2 verschiedene!)
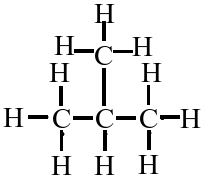
C4H10O
(mind. 2 verschiedene!)
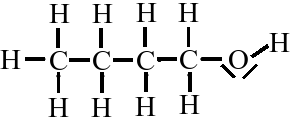
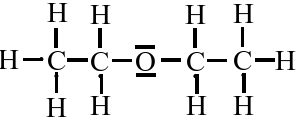
Zum Aufstellen einer Elektronenformel einer Verbindung, müssen
alle bindungsfähigen Elektronen der möglichen
Bindungspartner so miteinander verknüpft werden, dass kein
bindungsfähiges Elektron übrig bleibt! Es können
Kombinationen von Einfachbindungen und Zweifachbindungen oder
Dreifachbindungen auftreten. Die Bindigkeit jedes einzelnen Atoms
darf nicht überschritten werden! Die bindenden und die freien
Elektronenpaare sind am Ende so um ein Atom anzuordnen, dass sie
möglicht gleichmäßig voneinander entfernt sind
(Ausnahme: Doppelbindungen und Dreifachbindungen).
Zu beachten ist
dabei auch, dass keine Ringe mit weniger als 5 Atomen auftreten
dürfen!
Übung: versucht die Elektronenformeln zu erstellen von
|
H2O |
|
|
|
H2CO3 |
|
|
|
C2H6O |
|
|
|
C6H12 |
|
|
|
C2H2 |
|
|
|
CH4N2O |
|
|
|
C4H10 |
|
|
|
C4H10O |
|
|
Zur Erinnerung:
C ist immer 4-bindig und kann Einfach-,
Zweifach- und Dreifachbindungen,
N ist immer 3-bindig und kann
Einfach-, Zweifach- und Dreifachbindungen,
O ist immer 2-bindig
und kann Einfach-, und Zweifachbindungen,
H ist immer 1-bindig und
kann nur Einfachbindungen!